通常,固體物質的溶解度會因溫度的升高而逐漸增加,如硝酸鉀。但也有少數固體,如氫氧化鈣,其溶解度在溫度升高鄂同時卻是呈減小趨勢變化的。其溶解度曲線如圖(1)所示:
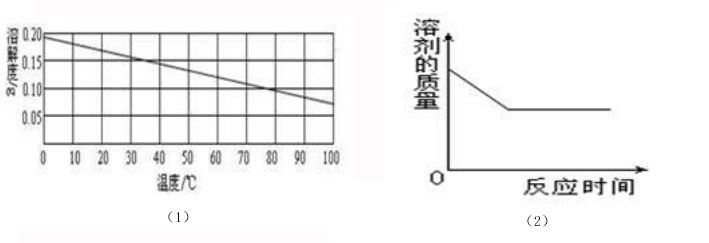
因氫氧化鈣溶解度會因溫度變化而減小,在某些問題上就需要我們特別注意。在實際操作中,若將一定量的生石灰加入到一定量的飽和氫氧化鈣溶液中,從反應的較初到反應結束,溶液的溫度變化規律是先升至一定溫度,然后又恢復到原來溫度的。在這個變化過程中,溶質的及溶劑、溶液的質量,溶液中溶質的質量分數、溶液中Ca2+的數目、溶液的PH的變化情況是怎樣的,具體情況如下:
一定溫度下,加入生石灰的氫氧化鈣溶液在特定時間內會放出大量的熱,令溶液的溫度升高,同時因為水的消耗而導致溶液內水質量減少。此時就會看出有部分的溶質氫氧化鈣被析出,令溶液內溶質質量減少。過一段時間,當溶液溫度逐漸降低時,在某一點被析出的氫氧化鈣有少部分將重新被溶解,具體情況如圖(2)所示,隨著反應時間的變化,溶劑的質量是先出現降低后持續不變。
以上變化中,雖然溶質的質量有所減少,其Ca2+總數也會減少,但是Ca2+的質量分數是不變的,因此氫氧化鈣溶液的堿性強弱是沒有變化的,即溶液的pH值不變。
在熟知以上變化的情況下,對于氫氧化鈣設備的實際運行來講是非常有利的。更多有關氫氧化鈣的介紹詳見:http://www.iferv.com/news